Badanie EuroPainClinics® Study I
Celem projektu EPCS I jest porównanie stanu klinicznego pacjentów, którzy po spełnieniu kryteriów wskazań poddali się terapii PRT.
Badanie EuroPainClinics®Study I (EPCS I) skupia się na badaniu klinicznym metody leczenia terapią PRT jako leczenia zespołów korzeniowych spowodowanych uciskiem korzenia nerwowego następstwem różnych procesów patologicznych, który powoduje tzw. ból korzeniowy. Najczęściej dotyczy to pacjentów, którym na podstawie tomografii komputerowej i rezonansu magnetycznego zdiagnozowano protruzję, przepuklinę lub wypadnięcie krążka międzykręgowego. Badanie skupia się na obserwacji długotrwałej ulgi w bólu i poprawy jakości życia pacjentów, którzy poddają się terapii PRT.
Dnia 23.4.2015 r. badanie zostało zatwierdzone przez regionalną szpitalną komisję etyczną pod numerem EK: 74/EK/15. Następnie zostało zarejestrowane w międzynarodowej bazie danych National Health Service USA https://clinicaltrials.gov PRS: NCT02464553.  EPCS 1 Approval document
EPCS 1 Approval document
Projekt spełnia wszystkie atrybuty i wiążące normy prawne dotyczące zabiegu medycznego zatwierdzonego przez Ministerstwo Zdrowia w Republice Słowackiej i Czeskiej.
Szczegóły badania
Badanie EuroPainClinics®Study I (EPCS I) skupia się na badaniu klinicznym metody leczenia terapią PRT
Terapia PRT – kryteria wskazań
PRT skupia się na leczeniu zespołów korzeniowych spowodowanych uciskiem korzenia nerwowego następstwem różnych procesów patologicznych. PRT to jedna z metod leczenia, przy której w pobliżu korzenia nerwowego iniekcyjnie podaje się przeciwzapalne leki razem z miejscowym znieczuleniem. Ból korzeniowy (ból spowodowany podrażnieniem rdzeniowych korzeni nerwowych) najczęściej spowodowany jest uciskiem korzeni w kanale kręgowym. Ucisk może być powodowany przez różne stany, takie jak zwężenie foraminal, zwężenie kanału kręgowego lub pooperacyjne zwłóknienie nadtwardówkowe w przestrzeni nadtwardówkowej itp.
Najczęściej dotyczy to pacjentów, którym na podstawie tomografii komputerowej lub rezonansu magnetycznego zdiagnozowano protruzję, przepuklinę lub wypadnięcie krążka międzykręgowego. Jeżeli u pacjenta ze zdiagnozowanym bólem korzeniowym ból utrzymuje się przez okres dłuższy niż 3 miesiące pomimo leczenia farmakologicznego i fizjoterapii, w następnym kroku po spełnieniu kryteriów wskazań zostaje wskazana terapia PRT. Jej celem jest uśmierzenie bólu i stanów zapalnych w obszarze korzenia nerwowego.
Należy pamiętać, że nie przy każdym stanie powodującym ucisk korzenia rdzeniowego można wykonać PRT. Przykładowe przeciwwskazania to wolny sekwestr (odłamek), nowotwory złośliwe, poważne ostre lub chroniczne choroby zapalne, koagulopatia itp.
Przedmiot badania EPCS I i rejestracja
Badanie EPCS I skupia się na obserwacji długotrwałej ulgi w bólu i poprawy jakości życia pacjentów, którzy poddają się terapii PRT i spełniają niżej wymienione kryteria wskazań w celu włączenia do badania.
Przedmiotem projektu jest realizacja wieloośrodkowego randomizowanego badania klinicznego z podwójnie ślepą próbą zajmującego się porównywaniem dwóch procesów metodycznych wykonania terapii PRT. Badanie zostało przygotowane i wypracowane przez organizację Europainclinics z.ú. Po wypracowaniu projektu badania, przygotowaniu świadomych zgód dla jego uczestników i wykonaniu protokołu badanie dnia 23.4.2015 r. zostało zatwierdzone przez regionalną szpitalną komisję etyczną pod numerem EK: 74/EK/15, Następnie zostało zarejestrowane w międzynarodowej bazie danych National Health Service USA
https://clinicaltrials.gov PRS: NCT02464553.
Projekt spełnia wszystkie atrybuty i wiążące normy prawne dotyczące zabiegu medycznego zatwierdzonego przez Ministerstwo Zdrowia w Republice Słowackiej i Czeskiej. Przetwarzanie danych osobowych pacjentów w celu przeprowadzenia badania wykonywane jest w zgodzie ze współczesną wersją Deklaracji Helsińskiej z 2008 r. i jednocześnie w zgodzie ze stosownymi ustawami danego kraju. Ochrona danych osobowych pacjentów zostanie zachowana. Dane będą przetwarzane według wymogów dyrektyw UE: dyrektywa 95/46/WE, dyrektywa 2002/58/WE, dyrektywa 2006/24/WE. Zostanie zapewnione, żeby protokół badania, świadome zgody z zabiegiem interwencyjnym i z włączeniem do odbywającego się badania zostały według miejscowych wymogów przedstawione stosownej niezależnej komisji etycznej. Jeżeli wymagają tego ustawy danego kraju, organizacja EuroPainClinics z.ú. poniesie odpowiedzialność za coroczne przedstawienie aktualizacji dokumentacji niezależnej komisji etycznej. Wyniki osiągnięte w badaniu zostaną opublikowane w międzynarodowych periodykach specjalistycznych i uwzględnione
Przebieg badania EPCS I
Badanie porównuje dwie grupy pacjentów z rozpoznaniem patologicznym na odcinku lędźwiowo-krzyżowym, u których wskazana jest terapia PRT. Warunkiem włączenia do badania jest wykrycie na rezonansie magnetycznym ucisku w jednej przestrzeni kręgowej, podczas gdy poziom symptomatologii klinicznej odpowiada dermatomu znajdującemu się o poziom niżej niż uszkodzenie.
Pacjent spełniający kryteria na włączenie do badania zostanie poinformowany przez lekarza przeprowadzającego badania lekarskie o prowadzonym badaniu i zostanie mu zaproponowana możliwość uczestnictwa. W razie zgody na uczestnictwo pacjent zostanie pouczony o interwencyjnej terapii PRT i następnie podpisze świadomą zgodę na obserwowane badanie i świadomą zgodę na inwazyjną terapię PRT w zakresie jednej lub dwóch przestrzeni międzykręgowych. Pacjent nie będzie wiedział, której z dwóch terapii zostanie poddany. Pacjent natomiast zgadza się na to, że szczegółowych informacji o prowadzonym badaniu dowie się dopiero po zakończeniu badania.
Pacjent jednak może w każdej chwili zażądać szczegółowe sprawozdanie o prowadzonej terapii. W takim wypadku natychmiast zostaną mu udostępnione wszystkie dane dotyczące dotychczasowego procesu leczniczego. Jednocześnie będzie wykluczony z obserwowanej grupy badania pacjentów. Pacjentowi zostanie przydzielony numer identyfikacyjny wygenerowany generatorem liczb losowych. Po wypełnieniu pierwszego protokołu z badania lekarskiego przed terapią zostanie wysłany protokół do koordynatora badania i do osoby, której powierzono przetwarzanie danych dotyczących badania. Pierwsze i drugie badanie pooperacyjne pacjenta wykona inny lekarz (niewykonujący tej terapii), odpowiednio inna placówka algezjologiczna i ponownie będą wypełnione protokoły z badań lekarskich.
Pacjenci spełniający kryteria zostaną losowo podzieleni na grupy A i B, przy czym pacjenci przydzieleni do grupy A będą poddani zabiegowi małoinwazyjnemu, podczas którego zostanie wykonana terapia PRT w jednej przestrzeni międzykręgowej. Pacjenci przydzieleni do grupy B będą poddani zabiegowi małoinwazyjnemu, podczas którego zostanie wykonana terapia PRT w dwóch sąsiadujących przestrzeniach międzykręgowych.
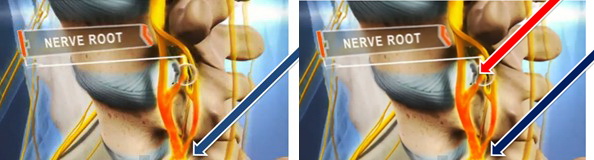
- Pacjenci przydzieleni do grupy A – 1: ostrzykiwanie nerwu w miejscu odpowiadającym symptomatologii
- Pacjenci przydzieleni do grupy B – 2: ostrzykiwanie nerwu w miejscu odpowiadającym symptomatologii i w miejscu ucisku korzenia weryfikowanego MR
Pierwsze kontrolne badanie pooperacyjne zapewni koordynator badania po 6 miesiącach i drugie kontrolne badanie pooperacyjne po 12 miesiącach.
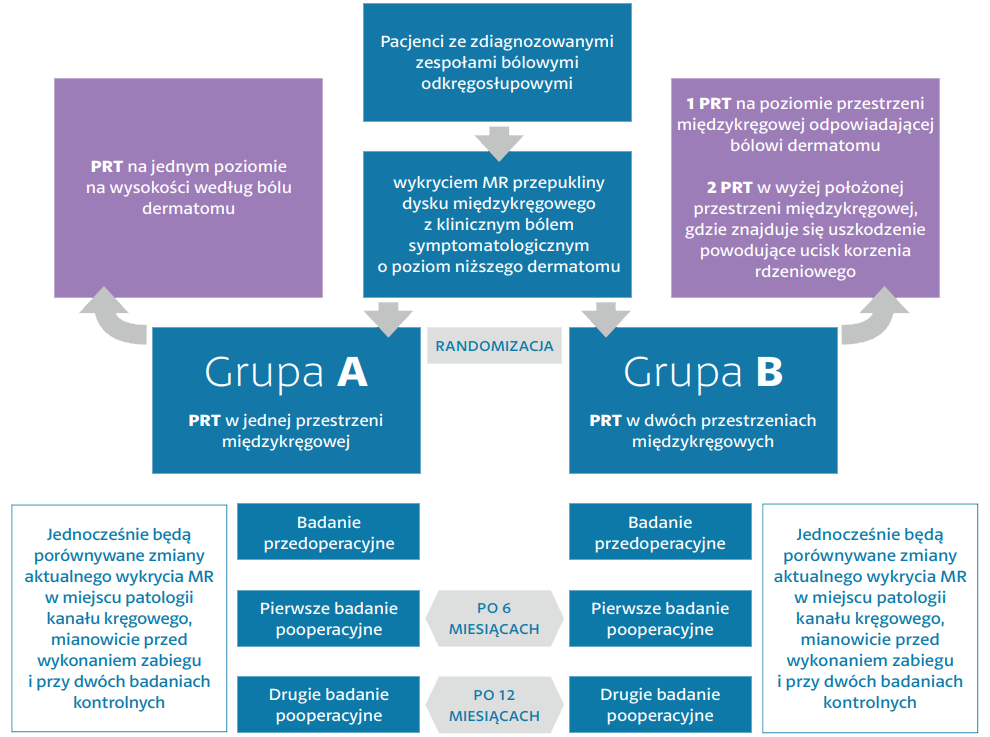
EPCS I study diagram
Cele badania EPCS I i obserwowane parametry
Celem projektu jest porównanie stanu klinicznego pacjentów, którzy po spełnieniu kryteriów wskazań poddali się terapii PRT i zostali przydzieleni do badania EPCS I. Obserwowane parametry będą wykorzystane do porównywania stanu klinicznego, wizualnego zakresu bólu, ogólnego wyniku na skali bólu, szerzenia bólu w odpowiednich dermatomach, obniżenia zużycia analgetyków oraz kwestionariusza Oswestry (oceniającego jakość życia pacjentów z bólem odcinka lędźwiowo-krzyżowego kręgosłupa). Obserwowane parametry będą odnotowywane w trzech przedziałach czasowych – przed zabiegiem (pierwsze badanie lekarskie), następnie 6 miesięcy po zabiegu (drugie badanie lekarskie) i ostatecznie 12 miesięcy po zabiegu (trzecie badanie lekarskie). Następnie wyniki będą poddane analizie statystycznej. Kolejny cel projektu to opublikowanie wyników w międzynarodowych periodykach specjalistycznych.
